Bộ Y tế thu hồi toàn quốc 6 loại mỹ phẩm nổi tiếng
Cục Quản lý Dược thu hồi 45 số công bố mỹ phẩm, trong đó 6 sản phẩm Derma Peel và Derma+ của Công ty TNHH Trinh Mỹ bị đình chỉ lưu hành toàn quốc.
Báo Znews đưa tin với tiêu đề: "Bộ Y tế thu hồi toàn quốc 6 loại mỹ phẩm nổi tiếng", nội dung được đăng tải như sau:
Ngày 28/1, Cục Quản lý Dược (Bộ Y tế) ban hành quyết định thu hồi 39 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm đã cấp cho nhiều doanh nghiệp trong nước, theo hình thức tự nguyện.
Theo Quyết định do Phó cục trưởng Cục Quản lý Dược Tạ Mạnh Hùng ký ban hành, việc thu hồi căn cứ trên đề nghị của các doanh nghiệp sở hữu sản phẩm, với lý do không còn nhu cầu tiếp tục kinh doanh các mặt hàng mỹ phẩm đã được công bố.
Cụ thể, 8 doanh nghiệp có sản phẩm bị thu hồi số tiếp nhận Phiếu công bố mỹ phẩm gồm: Công ty TNHH Mộc Thiền Sinh Thái; Công ty TNHH Thương mại Xuất nhập khẩu Hiếu Khánh; Công ty TNHH Mỹ phẩm Quốc tế Oly White; Công ty TNHH Tập đoàn BYC Japan Cosmetics; Công ty CP Dược phẩm Đại Phúc Long; Công ty TNHH Phân phối Liên hợp Đông Dương; Công ty TNHH Thương mại Dịch vụ và Sản xuất Mỹ phẩm Thúy Nga; Công ty TNHH Thương mại Xuất nhập khẩu Hóa mỹ phẩm BIG V.
Trong số 39 sản phẩm bị thu hồi, có nhiều dòng mỹ phẩm chăm sóc da, chống nắng, dưỡng trắng, trị mụn, serum, kem dưỡng, mặt nạ… từng được cấp số tiếp nhận trong giai đoạn từ năm 2021 đến 2025. Một số nhãn hàng quen thuộc xuất hiện trong danh sách như Yume Yume, Missbe, A-White, BYC JP, HEMIA, MINOYA, BIG V.
Quyết định có hiệu lực kể từ ngày ký ban hành. Danh mục chi tiết 39 số tiếp nhận Phiếu công bố mỹ phẩm bị thu hồi đã được cơ quan này đăng tải công khai trên trang thông tin điện tử của đơn vị để người tiêu dùng và các cơ quan liên quan theo dõi, giám sát.
Cùng ngày, Cục Quản lý Dược cũng quyết định thu hồi 6 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm do đơn vị này cấp cho các sản phẩm do Công ty TNHH Trinh Mỹ chịu trách nhiệm đưa ra thị trường. Đồng thời, cơ quan quản lý cũng yêu cầu đình chỉ lưu hành, thu hồi và tiêu hủy toàn quốc các sản phẩm này.
Các sản phẩm bị thu hồi mang nhãn hiệu Derma Peel và Derma+, gồm kem dưỡng, dung dịch làm sáng da, sữa rửa mặt tạo bọt và mặt nạ, được sản xuất tại Hàn Quốc. Trong đó, 5 sản phẩm do Chosung Corporation Co., Ltd và 1 sản phẩm do Rainbow Beauty Cosmetics Co., Ltd sản xuất. Số tiếp nhận Phiếu công bố được cấp từ năm 2021 đến 2025. Danh sách chi tiết 6 sản phẩm gồm:
- Dermapeel Rejuvenate
- Dermapeel-Max Brightening Stem Cell Solution
- Dermapeel Peptide Waterful Cream
- Dermapeel One-Touch
- Dermapeel 02 Bubble Foam Cleanser
- Derma+ Soothing Mask
-
Sản phẩm Derma+ Soothing Mask. Ảnh: Celinebeautymyths.
Lý do thu hồi, theo Cục Quản lý Dược, là hồ sơ thông tin sản phẩm (PIF) không đầy đủ và công thức mỹ phẩm không đúng với hồ sơ đã công bố. Trước đó, Sở Y tế TP.HCM đã xử phạt vi phạm hành chính Công ty TNHH Trinh Mỹ liên quan đến các sản phẩm này.
Cục Quản lý Dược yêu cầu các Sở Y tế thông báo tới cơ sở kinh doanh, sử dụng mỹ phẩm ngừng ngay việc kinh doanh và sử dụng 6 sản phẩm nêu trên, đồng thời tổ chức thu hồi, kiểm tra, giám sát và xử lý vi phạm.
Công ty TNHH Trinh Mỹ phải gửi thông báo thu hồi đến các đơn vị phân phối, tiếp nhận sản phẩm trả lại và báo cáo kết quả thu hồi về Cục Quản lý Dược trước ngày 5/3/2026. Sở Y tế TP.HCM được giao nhiệm vụ giám sát việc thu hồi và tiêu hủy, đồng thời báo cáo kết quả trước ngày 20/3/2026.
Cục Quản lý Dược cũng thông báo tạm ngừng xem xét và tiếp nhận hồ sơ công bố sản phẩm mỹ phẩm của Công ty TNHH Trinh Mỹ trong 6 tháng, căn cứ Thông tư số 06/2011/TT-BYT và các quyết định xử phạt trước đó. Trong thời gian này, cơ quan sẽ không tiếp nhận bất kỳ hồ sơ công bố sản phẩm mỹ phẩm nào đứng tên doanh nghiệp.
Báo Đời Sống Pháp Luật đưa tin với tiêu đề: "NÓNG: Thu hồi, tiêu huỷ 77 loại mỹ phẩm bao gồm nhiều dầu gội, sữa tắm, kem chống nắng nổi tiếng", nội dung được đăng tải như sau:
Cục Quản lý Dược thu hồi toàn quốc 77 mỹ phẩm của Ucanrely, gồm Pantene, Ichikami, Softymo, Tsubaki; Công ty Pharmedic bị xử phạt 70 triệu đồng vì vi phạm chất lượng.
Theo Tạp chí Tri thức, ngày 20/1, Cục Quản lý Dược (Bộ Y tế) ban hành quyết định đình chỉ lưu hành, thu hồi và tiêu hủy hàng loạt sản phẩm mỹ phẩm do Công ty TNHH Ucanrely đứng tên công bố. Quyết định được đưa ra căn cứ Nghị định 117/2020/NĐ-CP, Nghị định 124/2021/NĐ-CP, Thông tư 06/2011/TT-BYT về quản lý mỹ phẩm và kết quả kiểm tra của Cục Quản lý Dược.
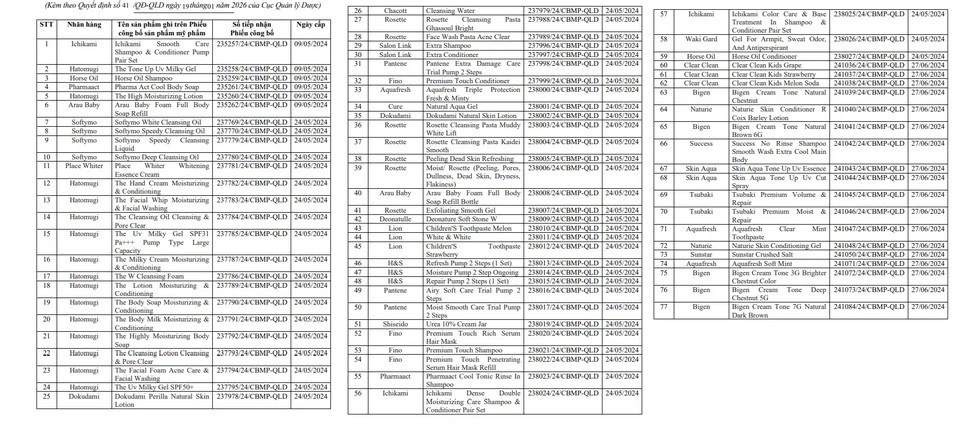
77 Phiếu công bố sản phẩm mỹ phẩm bị thu hồi
Nguyên nhân thu hồi là doanh nghiệp không xuất trình được Hồ sơ thông tin sản phẩm (PIF) theo quy định pháp luật. Quyết định cũng thu hồi số tiếp nhận Phiếu công bố mỹ phẩm của công ty này.
Cục Quản lý Dược yêu cầu Sở Y tế các tỉnh, thành phố: thông báo các cơ sở kinh doanh, ngừng lưu hành, sử dụng sản phẩm, tiến hành thu hồi và tiêu hủy theo quy định; đồng thời giám sát, kiểm tra và xử lý các đơn vị vi phạm.
Các sản phẩm bị thu hồi lần này của Công ty TNHH Ucanrely gồm 77 Phiếu công bố sản phẩm mỹ phẩm, trải dài nhiều nhóm mỹ phẩm, từ dầu gội, dầu xả, sữa tắm, kem dưỡng da, kem chống nắng, đến chăm sóc răng miệng. Các thương hiệu nổi tiếng như Ichikami, Hatomugi, Shiseido, Pantene, Softymo, Rosette, Fino, Tsubaki, Skin Aqua, Arau Baby, Aquafresh.

Đáng chú ý, nhiều sản phẩm thuộc dòng chăm sóc da và tóc Nhật Bản như Hatomugi The Tone Up UV Milky Gel, Ichikami Smooth Care Shampoo & Conditioner, Softymo Deep Cleansing Oil vốn được nhiều người tiêu dùng Việt sử dụng. Ngoài ra, các sản phẩm dành cho trẻ em như Arau Baby Foam Full Body Soap, Lion Children’s Toothpaste cũng nằm trong diện thu hồi.
Cục Quản lý Dược yêu cầu các cơ sở kinh doanh và người tiêu dùng không sử dụng các sản phẩm trên, đồng thời các sản phẩm phải được thu hồi và tiêu hủy toàn bộ. Thời hạn báo cáo kết quả thực hiện cho Cục Quản lý Dược là trước ngày 25/01/2026.
Công ty TNHH Ucanrely có trách nhiệm phối hợp với cơ quan quản lý để thực hiện đầy đủ các biện pháp khắc phục hậu quả theo quy định.

Thu hồi giấy phép Dược phẩm Hà Nội, phạt Pharmedic
Cùng ngày, Bộ Y tế cũng vừa ra quyết định xử phạt hành chính 70 triệu đồng đối với Công ty cổ phần dược phẩm dược liệu Pharmedic do vi phạm chất lượng trong sản xuất thuốc Diclofen (Diclofenac natri 50 mg), số lô 0040724, ngày sản xuất 26/7/2024, hạn sử dụng 26/7/2027.
Từ đầu tháng 1 đến nay, hàng loạt mỹ phẩm kém chất lượng, chứa các chất cấm hoặc chất không được công bố trong thành phần, không có số đăng ký... bị Cục Quản lý Dược thu hồi và tiêu hủy. Hôm 20/1, ba loại nước rửa tay, kem rửa mặt bán phổ biến trên thị trường bị thu hồi do chứa natri benzoate không có trong thành phần công thức sản phẩm. Tuần trước, 8 sản phẩm mỹ phẩmcũng bị thu hồi do chứa Miconazole, hoạt chất kháng nấm đã bị loại khỏi danh mục được phép sử dụng trong mỹ phẩm.
Trong bối cảnh cận Tết, nhu cầu chăm sóc sức khỏe và làm đẹp tăng cao, các cơ quan chức năng tăng cường kiểm tra đơn vị kinh doanh sản phẩm mỹ phẩm và kiểm soát thị trường để đảm bảo an toàn về chất lượng.
Công ty Pharmedic có trụ sở chính tại 367 Nguyễn Trãi, TP.HCM, do ông Lê Việt Hùng, Tổng Giám đốc, làm đại diện theo pháp luật. Lô thuốc Diclofen vi phạm chất lượng mức độ 2, được xác định theo quy định pháp luật.
Ngoài phạt tiền, Cục Quản lý Dược buộc công ty tiêu hủy toàn bộ lô thuốc vi phạm, mọi chi phí do doanh nghiệp chịu trách nhiệm. Công ty phải nộp số tiền phạt 70 triệu đồng vào Kho bạc Nhà nước khu vực I trong vòng 10 ngày kể từ ngày nhận quyết định, hoặc sẽ bị cưỡng chế và tính thêm 0,05% mỗi ngày trên số tiền chưa nộp.
Quyết định cũng nêu rõ công ty có quyền khiếu nại hoặc khởi kiện hành chính theo quy định pháp luật. Cục Quản lý Dược giao Phòng Quản lý Chất lượng thuốc và Sở Y tế TP.HCM phối hợp giám sát việc thực hiện.
Cơ quan này cũng vừa ban hành quyết định thu hồi Giấy chứng nhận đủ điều kiện kinh doanh dược số 793/ĐKKDD-BYT, cấp ngày 3/1/2023 cho Công ty cổ phần dược phẩm Hà Nội.
Theo quyết định, doanh nghiệp có trụ sở chính tại số 170 đường La Thành, phường Ô Chợ Dừa, TP Hà Nội. Địa điểm kinh doanh đặt tại lô 15, khu công nghiệp Quang Minh, xã Quang Minh, TP Hà Nội. Người chịu trách nhiệm chuyên môn về dược là ông Nguyễn Phú Bình, dược sĩ đại học, có chứng chỉ hành nghề dược số 01576/HNO-CCHND do Sở Y tế Hà Nội cấp ngày 25/11/2013.
Công ty cổ phần dược phẩm Hà Nội được cấp giấy chứng nhận đủ điều kiện kinh doanh dược với loại hình xuất khẩu, nhập khẩu thuốc. Tuy nhiên, tại Công văn số 115/CV-DPHN ngày 1/12/2025, doanh nghiệp đã chủ động đề nghị thu hồi giấy chứng nhận do không tiếp tục hoạt động kinh doanh dược trong lĩnh vực xuất khẩu, nhập khẩu thuốc tại địa điểm đăng ký.
Trên cơ sở đó, Bộ Y tế quyết định thu hồi Giấy chứng nhận đủ điều kiện kinh doanh dược nêu trên. Quyết định có hiệu lực kể từ ngày ký ban hành, đồng thời Quyết định số 01/QĐ-BYT ngày 3/1/2023 của Bộ trưởng Bộ Y tế về việc cấp giấy chứng nhận cho Công ty cổ phần dược phẩm Hà Nội cũng hết hiệu lực.